Das Plattenepithelkarzinom, auch Spinaliom oder Stachelzellkrebs
Zuletzt aktualisiert: 07.02.2025 | Autor(in): Carola Berking
Wie häufig ist ein Plattenepithelkarzinom?
Jährlich werden in Deutschland über 40.000 Neuerkrankungen des Plattenepithelkarzinoms der Haut verzeichnet. Hierbei sind Männer häufiger als Frauen betroffen.
Das durchschnittliche Erkrankungsalter der Betroffenen liegt bei über 70 Jahren.
Wie entsteht ein Plattenepithelkarzinom?
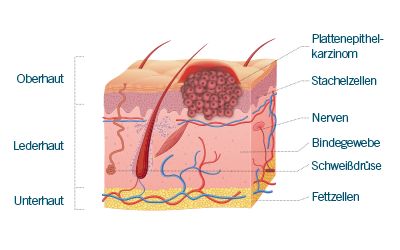
Das Plattenepithelkarzinom der Haut entsteht aus Keratinozyten (hornbildende Zellen) der Oberhaut (Epidermis), die aufgrund von Mutationen (Veränderungen im genetischen Code DNA) anfangen, unkontrolliert zu wachsen.
Bei dieser Hautkrebsart ist der Zusammenhang zwischen chronischer UV-Strahlung und Entstehung des Krebses am größten. Meist entsteht das Plattenepithelkarzinom auf schwer sonnenlichtgeschädigter Haut. Vorstufen sind die aktinische Keratose oder die Bowen-Krankheit (Morbus Bowen).
Was sind Vorstufen des Plattenepithelkazinoms?
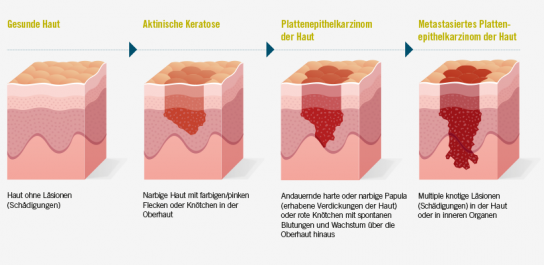
Bei den Vorstufen handelt es sich noch nicht um den voll ausgebildeten Krebs, da die schon in Richtung Bösartigkeit veränderten Zellen noch oberflächlich liegen und nicht die Grenze von der Oberhaut zur Lederhaut (Basalmembran) durchbrochen haben. Nicht jede Vorstufe muss sich in ein Plattenepithelkarzinom entwickeln, aber mit zunehmender Anzahl dieser Vorstufen erhöht sich auch das Risiko der Karzinomentstehung. Bei Diagnose einer aktinischen Keratose oder der Bowen-Krankheit wird daher empfohlen diese zu behandeln.
Das Plattenepithelkarzinom selbst wächst an der Stelle weiter, wo es entstanden ist. Zusätzlich können weitere Tumoren an anderen Stellen entstehen.
Wie ist der Verlauf der Erkrankung?
Der Verlauf des Plattenepithelkarzinoms kann sich von Fall zu Fall unterscheiden. Bei Immunsuppression (Unterdrückung des Immunsystems), beispielsweise durch Medikamente oder eine Infektionskrankheit, treten die Karzinome früher und häufiger auf und der Verlauf ist besonders aggressiv. Das betrifft besonders Patienten, die aufgrund einer Organtransplantation Medikamente einnehmen müssen, die das Immunsystem unterdrücken, damit das Transplantat nicht abgestoßen wird.
Wenn das Plattenepithelkarzinom nicht behandelt wird, kann es zum Einwuchs in tiefere Gewebeschichten kommen. In diesen Fällen können Knorpel, Knochen und Organe wie beispielsweise die Augen befallen werden. Dies führt zu Komplikationen und erfordert eine komplexere Behandlung.
5 % der diagnostizierten Plattenepithelkarzinome sind bereits fortgeschritten und können deshalb lebensgefährlich sein. Sie metastasieren in die Lymphknoten, Lungen oder ferner liegende Organe.
Tumore unter einer Größe von 1 cm haben sehr gute Heilungschancen. Wenn das Plattenepithelkarzinom nicht behandelt wird und fortschreitet, kann es schwer behandelbar werden und eine Gefahr darstellen.
Das Plattenepithelkarzinom der Haut, auch spinozelluläres Karzinom, Spinaliom, Stachelzellkrebs, Epithelioma spinocellulare oder Plattenepithelkrebs genannt, ist die zweithäufigste Hautkrebsart.
Tumore unter einer Größe von 1 cm haben sehr gute Heilungschancen.
Wenn das Plattenepithelkarzinom nicht komplett entfernt wird und fortschreitet, kann es schwer behandelbar werden und eine Gefahr darstellen.
- REFERENZEN
- Robert Koch-Institut, Gesellschaft der epidemiologischen Krebsregister in Deutschland e.V. (Hg.), Krebs in Deutschland 2013/2014. Häufigkeiten und Trends. 11. überarb. Auflage, Berlin 2017
- Leiter, U., et al. Incidence, mortality, and trends of nonmelanoma skin cancer in Germany. J Invest Dermatol;137:1860–7 (2017)
- Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): Aktinische Keratose und Plattenepithelkarzinom der Haut, Langversion 2.0, 2022, AWMF-Registernummer: 032/022OL
- Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): S3-Leitlinie Prävention von Hautkrebs, Langversion 2.1, 2021, AWMF Registernummer: 032/052OL
INTERESSENSKONFLIKTE
Symptome des Plattenepithelkarzinoms
Zuletzt aktualisiert: 03.02.2025 | Autor(in): Carola Berking
Vorstufe aktinische Keratose
Die Hautveränderung aktinische Keratose gilt als Vorstufe des Plattenepithelkarzinoms. Aktinische Keratosen fühlen sich wie Sandpapier an. Die Haut ist rauh mit rötlichen oder bräunlichen Flecken und leichter Schuppung oder Hornauflagerungen. Obwohl noch kein Krebs entstanden ist, wird empfohlen, die aktinische Keratose zu entfernen.
In manchen Fällen kann das Plattenepithelkarzinom auch aus Narben oder chronischen Wunden entstehen.
Entwicklung zum Krebs
Die Weiterentwicklung zum Krebs verläuft ohne klare Abstufungen: Es findet eine zunehmende Verhornung statt und der Tumor wächst nach oben und in die Tiefe. Oftmals haftet eine rötliche, braun-gelbliche Hornkruste fest. Sobald versucht wird, diese zu lösen, fängt sie an zu bluten.
Manchmal zeigt sich das Plattenepithelkarzinom als schorfige, verkrustete Wunde. Die betroffene Stelle ist oft empfindlich.
- REFERENZEN
- Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): S3-Leitlinie Prävention von Hautkrebs, Langversion 1.1, 2014, AWMF Registernummer: 032/052OLLetzter Zugriff: 04.06.2019
- Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): Aktinische Keratose und Plattenepithelkarzinom der Haut, Langversion 2.0, 2022, AWMF-Registernummer: 032/022OLLetzter Zugriff: 04.06.2019
- Dellavalle R. Skin cancer, moles, and actinic keratosis. In: Williams H, Bigby M, Herxheimer A, Naldi L, Rzany B, Dellavalle R (Ed). Edvidence-based dermatology. London: BMJ Books; 2014. S. 223-319
- Deutsche Krebshilfe, DKG: Die blauen Ratgeber, Hautkrebshttps://www.krebshilfe.de/infomaterial/Blaue_Ratgeber/Hautkrebs_BlaueRatgeber_DeutscheKrebshilfe.pdfLetzter Zugriff: 04.06.2019
INTERESSENSKONFLIKTE
Behandlung des Plattenepithelkarzinoms
Zuletzt aktualisiert: 07.02.2025 | Autor(in): Carola Berking
Die Behandlung des Plattenepithelkarzinoms ist abhängig von der Schwere der Erkrankung. Früh erkannte Plattenepithelkarzinome werden operiert und haben sehr gute Heilungschancen. Ist die Erkrankung bereits weiter fortgeschritten oder eine Operation nicht möglich, stehen weitere Behandlungsmöglichkeiten zur Verfügung.
Therapiemöglichkeiten beim Plattenepithelkazinom
Operation, die erste Wahl
Die in erster Linie empfohlene Standardtherapie ist die vollständige operative Entfernung des Tumors. Gerade kleinere Tumoren (unter 1 cm) können meist vollständig entfernt werden und haben sehr gute Heilungschancen.
Strahlentherapie
Als Alternative zur Operation kommt die Strahlentherapie in Frage, die auch postoperativ (nach einer Operation) bei Vorhandensein gewisser Risikomerkmale oder bei Rückfällen (Rezidiven) oder bei Inoperabilität (Operation nicht möglich aufgrund der Ausdehnung und Lokalisation des Tumors oder aufgrund des Zustands des Patienten) eingesetzt wird.
Immuntherapie
Beim lokal fortgeschrittenen oder metastasierten Plattenepithelkarzinom kommt als erste Option eine Immuntherapie mit Immuncheckpoint-Inhibitoren (PD1-Antikörpern) als bisher einzige zugelassene medikamentöse Therapie in Frage. Sie wird in Form von Infusionen im Abstand von 3-6 Wochen über mehrere Monate verabreicht.
Chemotherapie
Tumoren mit Lymphknotenbefall oder Metastasen in anderen Organen (z.B. Lunge) können mit Chemotherapie behandelt werden. In der Regel sprechen Plattenepithelkarzinome gut darauf an, allerdings kommt es häufig zu Rückfällen.
Elektrochemotherapie
Große knotige Tumoren oder tastbare Metastasen in der Haut können mit einer Elektrochemotherapie behandelt werden. Dabei wird örtlich eine Chemotherapie angewendet, die stark verdünnt als Infusion verabreicht und im Tumor hochkonzentriert aufgenommen wird durch das Auslösen von elektrischen Impulsen über Sonden, die der Chirurg in den Tumor unter laufender Narkose einsticht
Äußerlich anzuwendende Arzneimittel
Zur Behandlung von aktinischen Keratosen können äußerlich anzuwendende (topische) Arzneimittel zum Einsatz kommen. Dabei handelt es sich meistens um Cremes oder Gele, die regelmäßig auf die betroffene Stelle aufgetragen werden. Das Plattenepithelkarzinom selbst wird in der Regel nicht mit äußerlichen Arzneimitteln behandelt.
Das Plattenepithelkarzinom wird in erster Linie operativ entfernt. Ist eine Operation nicht möglich, wird häufig die Strahlentherapie eingesetzt. Im fortgeschrittenen Stadium kann mit systemischer medikamentöser (Chemo-)Therapie behandelt werden.
Abhängig von der Erkrankung kann z. B. auch mit Licht, Kälte oder anderen Verfahren behandelt werden.
- REFERENZEN
- Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): Aktinische Keratose und Plattenepithelkarzinom der Haut, Langversion 2.0, 2022, AWMF-Registernummer: 032/022OL
INTERESSENSKONFLIKTE
Systemtherapie des Plattenepithelkarzinoms
Zuletzt aktualisiert: 17.11.2025 | Autor(in): Ulrike Leiter-Stöppke
Für fortgeschrittene und metastasierte Plattenepithelkarzinome , die durch Lokaltherapie wie Operation oder Bestrahlung nicht mehr behandelbar sind, ist seit 2019 die Immuntherapie mit dem PD-1-Antikörper Cemiplimab zugelassen. Sie wird in Form von Infusionen im Abstand von 3 Wochen über mehrere Monate verabreicht. Mit diesem Medikament wird eine Ansprechrate von 44-50% mit einer langen Ansprechdauer erreicht (Median > 12 Monate)[1]. Das bedeutet, dass bei 44-50% der Behandelten ein teilweiser oder kompletter Rückgang des Tumors beobachtet wird. Ähnliche Ansprechraten zeigen Studien mit dem PD-1-Antikörper Pembrolizumab.
In aktuellen Studien wird der adjuvante[2] Einsatz von PD-1-Inhibitoren[3] bei Patienten mit Plattenepithelkarzinomen mit einem hohen Risiko für ein Wiederauftreten oder Fortschreiten der Erkrankung im Vergleich zu Placebo (= Scheinmedikament, ohne aktiven Wirkstoff) untersucht. Das bedeutet, dass im ersten Schritt das Plattenepithelkarzinom vollständig operativ entfernt wird. Im zweiten Schritt erhält der Patient einen PD-1-Inhibitor als Unterstützung, um das Risiko eines Rezidivs (= Wiederauftreten) zu senken. Die Ergebnisse der prospektiv randomisierten Phase 3 Studie an 412 Patienten, die nach einer Operation und anschließender Bestrahlung entweder Cemiplimab oder Placebo über ein Jahr erhalten haben, zeigten im Cemiplimab Arm eine Risikoreduktion von 68% ein Rezidiv zu entwickeln. Unter Cemiplimab bestand auch ein reduziertes Risiko, Lymphknotenmetastasen (80% ) bzw. Fernmetastasen (75%) zu entwickeln. Die Zulassung für die adjuvante Therapie wird Ende 2025 erwartet.
Eine internationale Studie zum neoadjuvanten Ansatz mit 79 Patienten wurde im September 2022 publiziert und im November 2023 mit einer längeren Nachbeobachtung aktualisiert. Hier wurden 4 Zyklen Cemiplimab vor der geplanten Operation verabreicht, um den Tumor gezielt vor der Operation zu verkleinern und eine Immunabwehr gegen den Tumor hervorzurufen. Hierbei zeigte sich bei 40 Patienten ein komplettes Ansprechen (es wurden nach Entfernen des Tumors keine vitalen Tumorzellen mehr nachgewiesen) und bei 10 Patienten ein partielles Ansprechen, d.h. es wurden im entfernten Tumorgewebe weniger als 10% vitale Tumorzellen nachgewiesen. Da 64% der Behandelten vom neoadjuvanten Einsatz der Anti-PD1-Therapie profitierten, wird dieser Ansatz in Zukunft eine interessante Therapieoption darstellen.
Die Kombination von Avelumab (PD-L1-Inhibitor) und dem EGFR-Inhibitor Cetuximab[4] wird derzeit in einer Studie bei inoperablen fortgeschrittenen Tumoren untersucht. Erste Ergebnisse sind vielversprechend, die Studie zeigte eine Stabilisierung bzw. ein Ansprechen von Patienten, die primär unter PD-1 Inhibitoren nicht angesprochen hatten.
Vor der Zulassung von Cemiplimab wurden verschiedene Chemotherapien und EGFR-gerichtete Antikörper alleine oder in Kombination eingesetzt. Daten aus Studien zu den medikamentösen Therapien sind in der u.g. Tabelle zusammengefasst. Für Patienten, die für eine Therapie mit Checkpointinhibitoren[5] nicht oder nur sehr eingeschränkt in Frage kommen (z.B. Organtransplantierte), werden diese Schemata empfohlen. Für diese Patienten gibt es bisher leider wenig neue therapeutische Entwicklungen.
[1] Median - Mittel- oder Zentralwert eines Datensatzes
[2] Adjuvante - ergänzende oder unterstützende Behandlungsmaßnahmen
[3] Inhibitor - (Hemm-)Stoff, der Reaktionen verlangsamt oder verhindert
[4] EGFR - Abkürzung von Englisch Epidermal Growth Factor Receptor (EGFR), ein Protein mit Signalwirkung in der Zelle
[5] Immuncheckpoint-Inhibitoren - Link/Verweis auf das Kapitel darüber resp. über ggf. Immuntherapien
| Therapie | Linie | Studienphase | Ansprechraten | Ansprechdauer (Median Monate) |
|---|---|---|---|---|
| PD1-Inhibitoren | Jede lokal fortgeschrittene bzw. metastasierte Tumoren | 2 | 34-50% | Nicht erreicht |
| EGFR-Inhibitoren | 1., 2. Lokal fortgeschrittene und metastasierte Tumoren | 1-2 | 28-45% | 6-8 |
| Chemotherapie* | 2 | 14-84% | 8,6-12 |
Für die Systemtherapie ist der PD-1-Antikörper Cemiplimab zugelassen, der ein gutes und langes Ansprechen zeigt. Dieser sollte als erste Therapiewahl angeboten werden.
Bei Fortschreiten (= Progress) unter Behandlung mit einem PD‐1‐Antikörper oder wenn ein PD-1-Antikörper nicht gegeben werden darf, stehen verschiedene Chemotherapien und EGFR-gerichtete Antikörper alleine oder in Kombination zur Verfügung.
Die adjuvante Therapie bei Hochrisikotumoren ergab eine Risikoreduktion für ein Rezidiv um 68% und wird Ende 2025 zugelassen.
Eine Studie zur neoadjuvanten Therapie zeigte einen hohen Nutzen mit einem nahezu kompletten Ansprechen bei 64% der Behandelten, so dass dies in Zukunft eine weitere Option darstellen könnte.
- REFERENZEN
- [1] Leiter U et. Al. (2020) S3 guideline for actinic keratosis and cutaneous squamous cell carcinoma (cSCC) - short version, part 2: epidemiology, surgical and systemic treatment of cSCC, follow-up, prevention and occupational disease. J Dtsch Dermatol Ges
- [2] Migden MR et. Al (2018) PD-1 Blockade with Cemiplimab in Advanced Cutaneous Squamous-Cell Carcinoma. N Engl J Med 379:341-351
- [3] Hillen U et al. (2018) Advanced cutaneous squamous cell carcinoma: A retrospective analysis of patient profiles and treatment patterns-Results of a non-interventional study of the DeCOG. Eur J Cancer 96:34-43
- [4] Gross ND, Miller DM, Khushalani NI et al. (2023) Lancet Oncol. Nov;24(11):1196-1205.
INTERESSENSKONFLIKTE
Tabelle zur Erklärung von Interessen und Umgang mit Interessenkonflikten
Nachsorge beim Plattenepithelkarzinom
Zuletzt aktualisiert: 03.02.2025 | Autor(in): Carola Berking
Die Nachsorge eines Plattenepithelkarzinoms der Haut beinhaltet regelmäßige Kontrolluntersuchungen durch einen Hautarzt. Dies dient der frühzeitigen Erkennung von Rückfällen oder neuen Hautveränderungen. Es ist wichtig, verdächtige Hautveränderungen selbst zu beobachten und dem Arzt mitzuteilen. Die Nachsorge ist an das Stadium der Erkrankung und somit an das individuelle Risiko angepasst.
Wie häufig erfolgen Nachsorgeuntersuchungen beim Plattenepithelkarzinom?
Die Intervalle der Nachsorge richten sich nach der Risikowahrscheinlichkeit, dass der Tumor an derselben Stelle wieder auftritt (Rezidiv) oder metastasiert.
Das Risiko ist bei jedem Patienten unterschiedlich. Es ist zum Beispiel davon abhängig, wie weit das Plattenepithelkarzinom fortgeschritten war, welche Behandlungsmethode gewählt wurde oder ob der Patient immunsupprimiert ist (das heißt wenn Medikamente eingenommen werden, die das Immunsystem unterdrücken, z. B. nach einer Organtransplantation).
Der behandelnde Arzt oder die Ärztin schätzt das Risiko für den Patienten ein und legt danach das Intervallschema fest. Es ist abhängig vom individuellen Risiko und vom Zurückliegen der Behandlung.
| Jahr 1–2 | Jahr 3–5 | Jahr 5–10 | |
|---|---|---|---|
| Geringes bis mittleres Risiko | 6-monatlich | jährlich | - |
| Hohes Risiko | 3-monatlich | 6-monatlich | jährlich |
Bei der Nachsorge des Plattenepithelkarzinoms ist es wichtig, die vorgesehenen Intervalle einzuhalten.
- REFERENZEN
- Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): Aktinische Keratose und Plattenepithelkarzinom der Haut, Langversion 2.0, 2022, AWMF-Registernummer: 032/022OLLetzter Zugriff: 04.06.2019
INTERESSENSKONFLIKTE
Link copied to clipboard!